FDA 승인 아세나핀 패치 (경피용 아세나핀)는 설하 아세나핀 연구에서 얻은 이전 효능 데이터와 607명의 성인 조현병 입원 환자를 대상으로 한 6주간의 중추적인 이중맹검, 위약 대조 임상시험을 통해 그 효능이 뒷받침되었습니다.경피 제형은 위약에 비해 1차(PANSS 점수) 및 2차(CGI-S 등급) 평가변수 모두에서 통계적으로 유의미한 개선을 보여 치료 효과를 확인했습니다.이러한 증거를 종합하여 조현병 치료에 대한 패치의 안전성, 효능 및 임상적 관련성을 입증했습니다.
주요 요점 설명:
-
설하 아세나핀의 효능 데이터
- 설하 아세나핀을 평가한 이전 임상시험은 조현병에서 약물의 작용 메커니즘과 치료 잠재력에 대한 기초적인 증거를 제공했습니다.
- 이러한 연구는 경피 제형의 용량, 안전성 프로파일, 예상 결과에 대한 정보를 제공하여 승인 경로를 간소화할 수 있었습니다.
-
중추적인 6주 이중맹검 임상시험
- 연구 디자인:607명의 참가자를 대상으로 한 엄격한 위약 대조 실험을 통해 강력한 통계적 힘을 확보하고 편향을 최소화했습니다.
- 모집단:임상 사용 대상 인구 통계를 반영하여 조현병 성인 입원 환자에 초점을 맞춥니다.
- 기간:6주간의 기간은 급성 증상 평가와 실제 임상 적용 가능성의 균형을 맞췄습니다.
-
1차 평가변수:PANSS 점수
- 양성 및 음성 증후군 척도(PANSS)는 조현병 증상의 중증도를 평가하는 표준 척도입니다.
- PANSS 점수가 통계적으로 유의미하게 개선되어 긍정적(예: 환각) 및 부정적(예: 사회적 금단) 증상을 모두 감소시키는 패치의 효능이 확인되었습니다.
-
2차 평가변수:CGI-S 평가
- 임상적 글로벌 인상-심각도(CGI-S) 척도는 임상의가 보고한 증상 개선에 대한 검증을 제공했습니다.
- 여기서 중요한 점은 환자별로 관찰 가능한 임상적 혜택을 강화했다는 점입니다.
-
안전성 및 내약성
- 참고 문헌에 명시적으로 설명되어 있지는 않지만, FDA의 승인은 경피 제형이 안전성 기준을 충족했음을 의미하며, 설하 데이터와 새로운 임상시험 부작용 보고를 활용했을 가능성이 높습니다.
- 경피 전달은 전신 부작용 감소(예: 경구 또는 주사제 경로 대비)와 같은 이점을 제공할 수 있습니다.
-
규제 근거
- FDA의 결정은 재현 가능한 효능(PANSS/CGI-S)과 통제된 임상시험 데이터로 뒷받침되는 명확한 위험-편익 프로파일에 달려 있습니다.
- 패치의 편의성 및 순응도 이점(예: 서방형, 비경구 경로)은 약물 순응도에 어려움을 겪는 인구 집단에 대한 승인을 더욱 정당화했을 수 있습니다.
의료 구매자에게는 이 증거가 다음을 강조합니다. 아세나핀 패치 는 투여 및 내약성 측면에서 잠재적인 이점이 있는 조현병 관리를 위한 실행 가능하고 근거가 뒷받침된 옵션입니다.경피 제형이 환자의 요구 사항이나 기관의 프로토콜에 부합할까요?
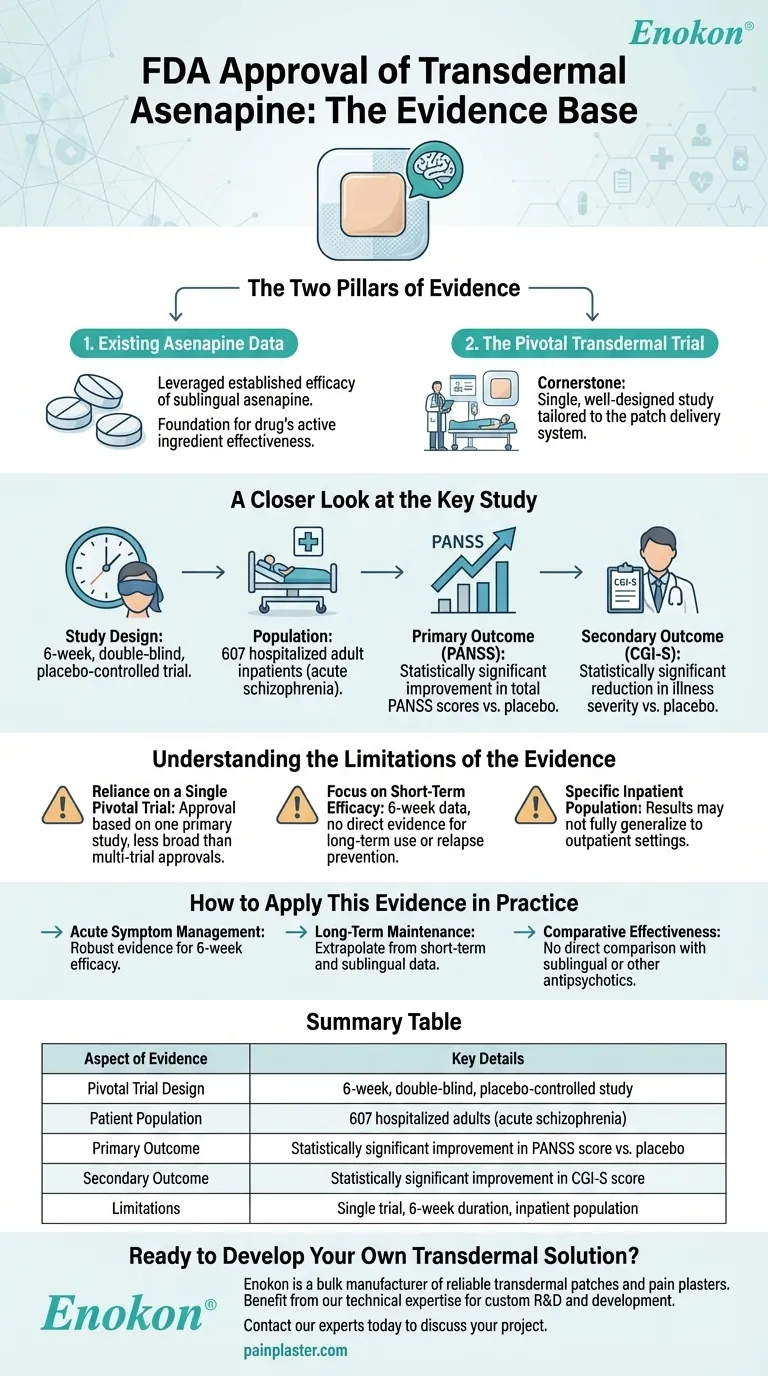
요약 표:
| FDA 승인을 위한 주요 증거 | 세부 정보 |
|---|---|
| 이전 설하 아세나핀 데이터 | 확립된 작용 기전 및 안전성 프로파일 |
| 중추적인 6주 임상시험 | 607명의 성인 정신분열증 입원 환자, 이중 맹검, 위약 대조군 |
| 1차 평가변수(PANSS 점수) | 통계적으로 유의미한 증상 감소 |
| 2차 평가변수(CGI-S 등급) | 임상의가 확인한 중증도 개선 효과 |
| 안전성 및 내약성 | FDA 벤치마크 충족, 잠재적 준수 혜택 |
| 규제 근거 | 재현 가능한 효능 및 명확한 위험-편익 프로파일 |
경피용 아세나핀을 귀사의 치료 프로토콜에 통합하는 데 관심이 있으신가요?
신뢰할 수 있는 경피 패치 및 통증 플라스터 대량 제조업체입니다, Enokon 은 헬스케어 유통업체와 제약 브랜드를 위한 신뢰할 수 있고 임상적으로 검증된 솔루션을 제공합니다.맞춤형 R&D에 대한 전문성을 바탕으로 환자의 니즈에 맞는 제형을 보장합니다.
지금 바로 문의하세요 에 문의하여 파트너십 기회를 논의하거나 제품 샘플을 요청하세요.
시각적 가이드
관련 제품
- 실리콘 흉터 시트 패치 경피 약물 패치
- 원적외선 열 통증 완화 패치 경피 패치
- 멘톨 젤 통증 완화 패치
- 아이시 핫 멘톨 약용 통증 완화 패치
- 목 통증에 대한 쑥 쑥 통증 완화 패치











